Esto es lo que peor se os dió
Blog de apoyo a las clases. Busca tu curso o el tema que te interesa en las ETIQUETAS.
martes, 19 de diciembre de 2017
miércoles, 13 de diciembre de 2017
Ejercicios de disoluciones 2ESO
Para realizar en el aula y de tarea en casa según lo vaya yo indicando,
Enlace al archivo, documento aquí
Enlace al archivo, documento aquí
miércoles, 6 de diciembre de 2017
Feliz puente
Os recuerdo que a la vuelta están las recuperación de la primera evaluación. Disfrutar y estudiar para terminar el año con todo aprobado
martes, 5 de diciembre de 2017
Tareas de 2ºESO
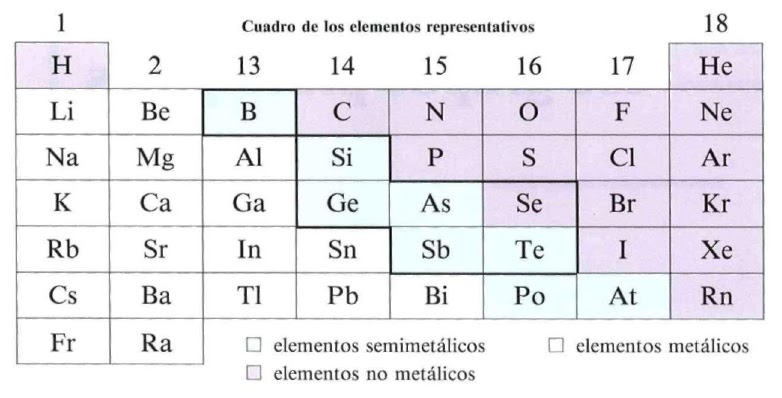
Aprender el sistema periódico, los elementos representativos, los que habéis copiado en la hoja del cuaderno. Grupos 1-2-13-14-15-16-17 (el 18, los gases nobles, no para ahora). Nos aprendemos el nombre de los grupos y cuales elementos son metales, no metales y semimetales (los colores que habéis puesto en vuestra tabla)

lunes, 4 de diciembre de 2017
SUSTANCIAS SIMPLES Y COMPUESTAS
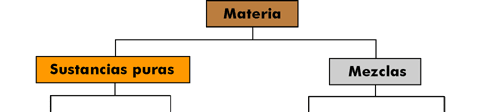
| Clasificación de la materia |
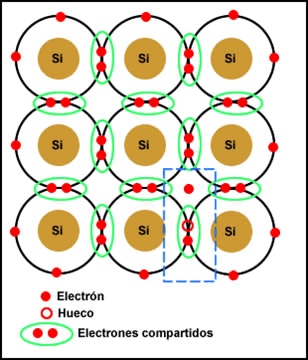
El tipo de partícula a que da lugar la unión de átomos depende precisamente de cuáles son esos átomos y de qué forma se unen, es decir, del enlace químico producido entre ellos.
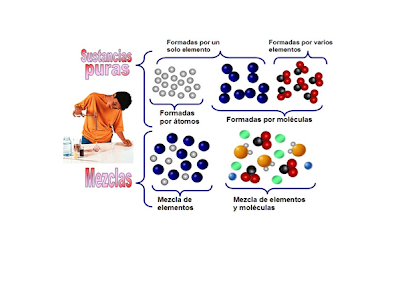
SUSTANCIAS SIMPLES: es aquella sustancia que esta formada por uno o mas átomos del mismo elemento químico
SUSTANCIAS COMPUESTAS: cuando la sustancia se puede descomponer mediante procesos quimicos
MEZCLA HETEROGENEA: es aquella en la que las partes mantienen propiedades intensivas diferentes
Trabajos de exposición de 2 ESO
- Radiactividad.
- Lluvia ácida.
- Efecto invernadero.
- Capa de ozono. Contaminación.
- Máquinas simples (palanca, polea, torno, plano inclinado). Utilidades.
- Formas de energía (cinética, potencial, electromagnética…).
- Energías renovables y no renovables.
- Centrales térmicas.
- Centrales nucleares.
- Centrales hidroeléctricas. Energía hidráulica.
- Centrales eólicas. Energía eólica.
- Centrales solares. Energía solar.
- Energía mareomotriz y energía geotérmica.
- Energía de la biomasa.
- Efectos medioambientales del consumo energético. Ahorro energético.
- Carbón, petróleo, gas natural, uranio. Fuentes de energía no renovables.
- Química, sociedad y medioambiente. Contaminación.
- Reciclaje. Contenedores…
Tipos de reacciones químicas
Las sustancias reaccionan entre sí de maneras muy diversas: el gran número de reacciones químicas que se producen justifica la necesidad de clasificarlas para su estudio.
Hay diferentes tipos de reacciones químicas y varias formas de clasificarlas según el criterio elegido. Los criterios que se siguen son generalmente cuatro: el energético, el cinético, la transformación que se produce y la partícula intercambiada.
Pincha en la imagen y tendrás información de cada uno de los tipos
 |
| Fuente :http://e-ducativa.catedu.es/44700165/aula/archivos/repositorio/1000/1169/html/index.html |
enlaces interesantes:problemas de estequiometria resueltos PARA SABER MAS
- Reacciones químicas. Cálculos. teoría y ejercicios tipo explicados
- CÁLCULOS ESTEQUIOMÉTRICOS ejercicios con solución
jueves, 30 de noviembre de 2017
Ej repaso para la recuperacion de la 1ev de 2eso
Ejercicios resueltos de densidad, para preparar el examen de recuperación de la 1º evaluación , enlace aquí
Cualquier duda, me la podéis preguntar en clase.
Haciendo ejercicios es como se aprende. Animo y a superar la recuperación.🔺
miércoles, 29 de noviembre de 2017
Ejercicios para los alumnos Pendientes de 3º (también de repaso para 4º que han suspendido la evaluación)
2º EVALUACIÓN_
Hacer para la siguiente clase
- Resumen de estos temas
TEMA 3 ESTRUCTURA DEL ÁTOMO
TEMA 4 ELEMENTOS Y COMPUESTOS (tabla periódica. enlaces )
- Los siguientes ejercicios en el cuaderno:
11 electrones.
b
) Razona su número átomico y su
número másico
c) Dibuja el átomo anterior
según Bohr
2.- a) Un ión posee 26 protones y 24 electrones. Razona si es anión o
catión
b) Un átomo tiene de nº
atómico 12, ¿cuántos electrones de valencia tiene?.
c) Escribe los nombres y símbolos de los
elementos situados en el grupo 15 del S .P.
d)¿Qué
nombre recibe dicho grupo?.¿Qué tienen en común?. ¿son metales o no metales?
3.- a) Define
isótopo
b)En la
naturaleza encontramos dos isótopos del cloro. Uno de sus isótopos, el Cloro
35, lo encontramos en una abundancia del 75,5 %. Si la masa media del elemento
cloro es de 35,5, calcula la masa atómica del otro isótopo.
4.-Realiza un esquema de la tabla periódica en el que venga indicado:
4.-Realiza un esquema de la tabla periódica en el que venga indicado:
a) Metales y no metales
b) Nombre de los grupos representativos.
c) Escribe los nombres y símbolos de los
elementos del grupo 15 del Sistema periódico.
d) Coloca razonadamente
los elementos que tienen las siguientes configuraciones externas y dí su
nombre: 1) 3s23p2 ;
2) 4s1 ; 3)
4s23d6 ; 4) 2s22p4 ; 5) 4s2 4p6 ; 6)
1s2
5.- a) Razonar el tipo de enlace que existe entre los siguientes átomos nombrando la sustancia
obtenida:
1) Bromo y Potasio
2) Azufre e hidrógeno
3) Átomos de calcio
b) Razona entre
las sustancias anteriores cuales son sólidos, gases, conducen la corriente
eléctrica o
se disuelven en agua
Os recuerdo este criterio fundamental para aprobar
Se considera imprescindible la entrega y correcta cumplimentación del guión de prácticas para aprobar la asignatura.
martes, 28 de noviembre de 2017
Examen de 4C
Traer solucionado para mañana, en tu cuaderno, con ayuda del libro de texto, enlace aquí
Vídeo estudio del sonido- 2º ESO
Lo veremos para analizar el contenido , más adelante cuando veamos la práctica 4º del cuaderno de laboratorio.
Ahora nos sirve para ver como se presenta un video de una práctica de laboratorio, en un enfoque de noticia, de relato periodístico de información científica, por aquellos que habéis decidido como trabajo extra una práctica de laboratorio.
Enlace al video aquí
Ahora nos sirve para ver como se presenta un video de una práctica de laboratorio, en un enfoque de noticia, de relato periodístico de información científica, por aquellos que habéis decidido como trabajo extra una práctica de laboratorio.
Enlace al video aquí
lunes, 27 de noviembre de 2017
jueves, 23 de noviembre de 2017
Corrección del 2º examen de evaluación
Estimados alumnos, para aprender de los errores, y como os dije en el aula, después de hacer el examen, se corrige en clase, y todo aquel que lo termine y complete , podrá ver el examen que hizo y apuntar sus errores para aprender. Pues, lo importante es aprender , y el que se lo sabe tendrá éxito en el examen,si este examen no ha sido superado , ya sabes lo que le falta y debes mejorar, así puedes preparar mejor la recuperación.
Por favor, ser consecuentes, la nota que sacáis es la que tenéis y yo soy la primera disgustada cuando no superáis el examen.
Por favor, ser consecuentes, la nota que sacáis es la que tenéis y yo soy la primera disgustada cuando no superáis el examen.
jueves, 16 de noviembre de 2017
4ESO-U8-soluciones a los ejercicios del tema
De tarea hacer los ejercicios indicados , cuya solución os pongo aquí abajo, en clase sólo me preguntáis las dudas de los que no os salen
HIDROCARBUROS
COMPUESTOS OXIGENADOS
martes, 14 de noviembre de 2017
lunes, 13 de noviembre de 2017
domingo, 12 de noviembre de 2017
jueves, 9 de noviembre de 2017
tema 2: la materia y sus estados de agregación
- Estados de la materia:
Este es el enlace que seguiremos en el aula para explicar el tema:
http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/indice.htm
- Ejercicios interactivos, extras, para aprender de otra forma, entra y apunta en tu cuaderno lo que observas:
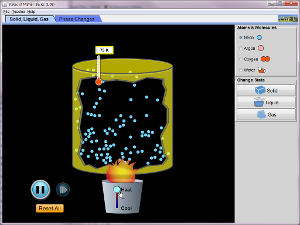
Estados de la Materia: Básico
| Calienta, enfría y comprime los átomos y moléculas y vea cómo ellos cambian entre sólido, líquido y fases gaseosas. |
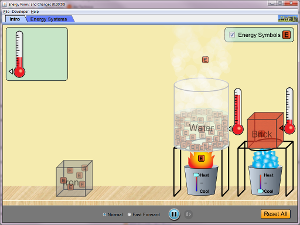
Cambios y formas de energías
| Explore how heating and cooling iron, brick, and water adds or removes energy. See how energy is transferred between objects. Build your own system, with energy sources, changers, and users. Track and visualize how energy flows and changes through your system. |
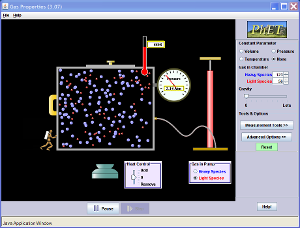
Propiedades del gas
| Bombea moléculas de gas en una caja y vea qué sucede a medida que cambia el volumen, añada o elimine el calor, cambia la gravedad, y mucho más. Mida la temperatura y la presión, y descubra cómo las propiedades del gas varían en relación con los demás. |
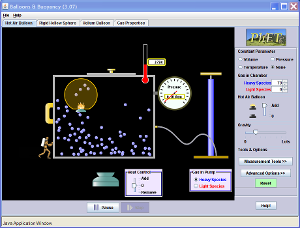
Globos y flotación
| Experimenta con un globo de helio, un globo con aire caliente, o una esfera rígida llenada con diferentes gases. Descubre lo que hace que algunos globos floten y otros se hunden. |
domingo, 5 de noviembre de 2017
U.7 El SISTEMA PERIÓDICO Y EL ENLACE QUÍMICO
El sistema periódico
La tabla periódica es la herramienta más importante y efectiva que utilizan los químicos para organizar y registrar información que alude a esta disciplina.En esta unidad estudiaremos y analizaremos la tabla periódica como marco para examinar propiedades tales como radio atómico, energía de ionización, afinidad electrónica, entre otras.- tabla periodica y la configuración electronica
- Aquí os dejo el enlace a la que usamos en el aula, es interactiva y nos viene para imprimir: http://periodni.com/es/#la
- Para estudiar una tabla muda interactiva que te califica: http://es.calcuworld.com/tabla-periodica-muda
http://quifi-mj.blogspot.com.es/2017/09/elementos-quimicos.html
http://quifi-mj.blogspot.com.es/2012/11/tabla-periodica-facil-aprender-estados.html
Actividades extraescolares 4º
Semana de la ciencia
| |||
Para informaros del Recorrido al Jardín Botánico os dejo los siguientes enlaces:
- http://www.botanicoalcala.es/files/recorrido1.pdf plano del recorrido que vamos a realizar.
- http://www.botanicoalcala.es/files/recorridogeneralesp.pdf explicación del mismo.
IMPORTANTE:
Haremos dos grupos de unos 22 alumnos, uno con cada pofesora,
LOS ALUMNOS ESTARÁN SIEMPRE EN EL GRUPO, QUE NO ABANDONAN ESTE Y QUE NO ENTRARÁN DENTRO DE LAS ZONAS DE PLANTACIÓN NI CORRERÁN DETRÁS DE CONEJOS, LIEBRES, PERDICES, ETC.
en el jardín Botánico hay esa fauna que te menciono gracias a la actitud de los visitantes, de tranquilidad y respeto, algo difícil para chicos de esa edad.
Además se debe cumplir lo siguiente: no hacerlo será un parte y estar excluido para cualquier otra excursión que se realice:
- No está permitida la recolección de plantas o partes de éstas, frutos, flores, semillas, hojas, etc., ni siquiera las partes que pudieran caer al suelo por sí mismas.
- No está permitido el paso fuera de los caminos o accesos habilitados.
- La conservación del jardín botánico no permite el paso de animales domésticos ni de vehículos salvo sillas de ruedas. Se trata de un parque de obligado recorrido a pie.
- No se permite la utilización del recinto como parque de juegos, celebración de encuentros, botellón, etc. TAMPOCO SE PERMITE UTILIZAR LAS ZONAS DE AULA AL AIRE LIBRE COMO MERENDEROS.
- No se debe molestar o perturbar a la fauna silvestre, por lo que se ruega transitar con tranquilidad y hacer el menor ruido posible. Tampoco se permite hacer fuego.
Deben recordar en todo momento que aunque parezca que están en el campo, al aire libre, están en un MUSEO, UN MUSEO DE PLANTAS Y ANIMALES VIVOS.
- No está permitido el paso fuera de los caminos o accesos habilitados.
- La conservación del jardín botánico no permite el paso de animales domésticos ni de vehículos salvo sillas de ruedas. Se trata de un parque de obligado recorrido a pie.
- No se permite la utilización del recinto como parque de juegos, celebración de encuentros, botellón, etc. TAMPOCO SE PERMITE UTILIZAR LAS ZONAS DE AULA AL AIRE LIBRE COMO MERENDEROS.
- No se debe molestar o perturbar a la fauna silvestre, por lo que se ruega transitar con tranquilidad y hacer el menor ruido posible. Tampoco se permite hacer fuego.
Deben recordar en todo momento que aunque parezca que están en el campo, al aire libre, están en un MUSEO, UN MUSEO DE PLANTAS Y ANIMALES VIVOS.
2eso_Tema2_Hacer estas dos semanas para preparar el 2º examen de la evaluacion
Estados de la materia. Cambios de estado.
 Ejercicios: Realiza de forma interactiva en el ordenador, se corrige de forma automática, y copias el resultado final en tu cuaderno .
Ejercicios: Realiza de forma interactiva en el ordenador, se corrige de forma automática, y copias el resultado final en tu cuaderno . - Estados de agregación: ejercicio I; ejercicio II
- Cambios de estado: ejercicio I y ejercicio II
- Gráficas de cambio de estado: ejercicio I; ejercicio II
martes, 31 de octubre de 2017
Ejercicios de refuerzo para los pendientes de 3ºESO para preparar el examen de la 1evaluación
1º EVALUACIÓN
TEMA 1 ACTIVIDAD CIENTÍFICA
TEMA 2 LA MATERIA. GASES Y DISOLUCIONES
Examen el jueves 16 de noviembre a las 14:15h
Para saber más y repasar conceptos básicos: Realiza los ejercicios que aparecen en el siguiente enlace, aqui
Tarea 2ESO A_Ej del Examen del tema 1
Realiza los ejercicios que aparecen en el siguiente enlace, aqui que son los del examen, como tarea en tu cuaderno.
viernes, 27 de octubre de 2017
miércoles, 18 de octubre de 2017
Rayos catódicos/Cathode rays
Aparatos para la enseñanza de las leyes físicas del siglo XIX
La llamada bobina de inducción o bobina de Ruhmkorff, de
invención anterior a la de los
transformadores de corriente alterna, es un verdadero
transformador polimorfo y elevador,
en el que se obtiene, a partir de una corriente primaria
continua y de poca fem (pilas o
acumuladores), otra de alta tensión y alterna.
Los cinco
tubos de Crookes de la colección permiten poner de manifiesto diversos efectos
y propiedades de los rayos catódicos y de los rayos canales.
Los tubos contienen gas altamente enrarecido, es decir, la presión de gas en el interior es extraordinariamente baja.
Los tubos contienen gas altamente enrarecido, es decir, la presión de gas en el interior es extraordinariamente baja.

Espectro electromagnético

Se denomina espectro electromagnético a la distribución energética del conjunto de las ondas electromagnéticas. Referido a un objeto se denomina espectro electromagnético o simplemente espectro a la radiación electromagnética que emite (espectro de emisión) o absorbe (espectro de absorción) una sustancia
martes, 17 de octubre de 2017
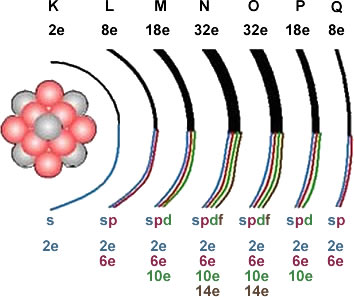
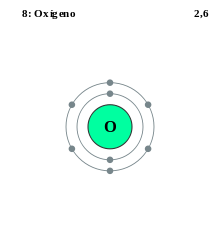
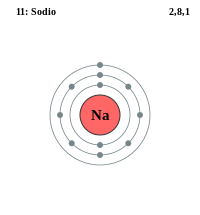
Configuracion electrónica
viernes, 13 de octubre de 2017
Peróxidos
- consisten en combinaciones binariasformados por la unión de un metal con el ion peróxido, -O-O-, O22-La fórmula de los peróxidos es del tipo X2(O2)n (donde X es el elemento metálico, O es oxígeno y n es la valencia del elemento metálico).formulan y nombran como los óxidos básicos sustituyendo el ion O2- de los óxidos metálicos por el ion O
 y la palabra óxido por peróxido.El subíndice 2 del ion peróxido no puede simplificarse.
y la palabra óxido por peróxido.El subíndice 2 del ion peróxido no puede simplificarse. - Li+1 + O2-2 » Li2O2: peróxido de lítio
- Cu+1 + O2-2 » Cu2O2: peróxido de cobre (I)
- Cu+2 + O2-2 » Cu2(O2)2 » CuO2: peróxido de cobre (II)
- Nomenclatura de stock: la nomenclatura de stock se realiza indicando el número de ox del elemento metálico entre paréntesis y en números romanos, precedido por la expresión "peróxido de" + elemento metálico.
Ejemplo:Cu2O2: peróxido de cobre (I)
Ti2(O2)3: peróxido de titanio (III)En el caso de aquellos elementos metálicos que sólo actúan con una valencia no es necesario indicarla.Ejemplo:Li2O2: peróxido de litio en lugar de peróxido de litio (I)Ojo - Peróxido de titanio (II)
- Ti+2 + O2-2 » Ti2(O2)2 » Ti(O2):
- dejamos los paréntesis para no confundir con óxido de titanio (IV)
- Nomenclatura sistemática:
- Para nombrar los peróxidos con la nomenclatura IUPAC, lo haremos como en los oxidos se indica mediante prefijos numéricos seguidos de la expresión óxido + el prefijo correspondiente junto al elemento metálico.K2O2 dióxido de dipotasio ( peróxido de potasio)CaO2, dióxido de calcio. ( peróxido de calcio)
miércoles, 11 de octubre de 2017
Tareas de 2ºESO
Añade la información del libro , pag25, diferenciando capacidad y volumen
- De los videos de cambio de unidad con factores de conversión , haz 5 de los ejercicios en tu cuaderno, fijate en los pasos, y si no te salen lo haces tal y como lo explican.
- Terminar las fichas de clase, que ya deberían estar hechas, pues las hemos ido haciendo en el aula, lo que falte se termina.
martes, 10 de octubre de 2017
P0-Reconocimiento de material de laboratorio
Si pinchas aquí hay la información, una presentación, para que estudies y seas capaz de reconocer el material de laboratorio, y saber su utilidad. Luego en el aula te preguntaré sobre ello.
Suscribirse a:
Entradas (Atom)



 Hacer un resumen, en una hoja aparte, de las paginas 210-211-212 del libro, y traerlo junto con el cuaderno de prácticas al laboratorio.
Hacer un resumen, en una hoja aparte, de las paginas 210-211-212 del libro, y traerlo junto con el cuaderno de prácticas al laboratorio.  copiar esta imagen del montaje para poder hacerlo en el laboratorio, la foto del cuadernillo se ve mal
copiar esta imagen del montaje para poder hacerlo en el laboratorio, la foto del cuadernillo se ve mal