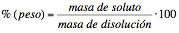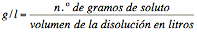Ejercicio de repaso:
El
médico te receta un medicamento que tiene una concentración de ácido
acetilsalicílico del 32%. ¿Qué cantidad de dicho ácido hay en un sobre de 500
mg????? Te recuerdo que lo primero es identificar el soluto y la disolución y luego aplicar la formula que en este caso será:
Las
disoluciones son
mezclas homogéneas de dos o más sustancias.
- El soluto es el componente que se encuentra en distinto estado físico que la disolución; y el disolvente es la sustancia que está en igual estado físico que la disolución. Cuando hay una ruptura de enlaces hay una reacción química y un cambio energético.
- El soluto puede ser un gas, un líquido o un sólido, y el disolvente
puede ser también un gas, un líquido o un sólido. El agua con gas es un
ejemplo de un gas (dióxido de carbono) disuelto en un líquido (agua).
Las mezclas de gases, como ocurre en la atmósfera, son disoluciones.
Las
disoluciones verdaderas se diferencian de las
disoluciones coloidales y
de las suspensiones en que las partículas del soluto son de tamaño
molecular, y se encuentran dispersas entre las moléculas del disolvente.
Observadas a través del microscopio,
las disoluciones aparecen homogéneas y
el soluto
no puede separarse por filtración. Las sales, ácidos y bases
se ionizan al disolverse en agua. Algunos metales son solubles en otros
en estado líquido y solidifican manteniendo la mezcla de átomos. Si en
dicha mezcla los dos metales pueden solidificar en cualquier proporción,
se trata de una disolución sólida llamada aleación.
Las disoluciones se caracterizan por tener una
fase homogénea, es decir, tiene las
mismas características en todos sus puntos,
o lo que es lo mismo: el aspecto, sabor, color, etc. son siempre los
mismos. Si una disolución está turbia ya no es una disolución; y existen
disoluciones de todos los estados físicos en todos los estados físicos
en todos los estados físicos.

Las disoluciones
se pueden clasificar según su concentración en:
Diluidas: En estas, hay muy poca cantidad de soluto, el disolvente puede seguir admitiendo más soluto.
Concentradas: En ellas hay bastantante cantidad de soluto disuelto, pero el disolvente todavía puede seguir admitiendo más soluto.
Saturadas:
Son aquellas que a una temperatura determinada no pueden seguir
admitiendo más soluto. Si la temperatura aumenta, la capacidad para
admitir más soluto aumenta.
Sobresaturadas: Son aquellas
que estando saturadas a una temperatura determinada, se aumenta esta
para poder echar más soluto, y se vuelve a bajar con cuidado para que no
precipite. Si se les añade más soluto o se mueve bruscamente,
precipita.
Formas de expresar la concentración
Indica la masa en gramos disuelta en cada litro de disolución. Tiene la ventaja de ser una concentración expresada en unidades directamente medibles para
el tipo de disoluciones más frecuentes en química (las de sólidos en
líquidos). La balanza expresa la medida de la masa de soluto en gramos y
los recipientes de uso habitual en química indican el volumen de
líquido contenido en litros o en sus submúltiplos. Su cálculo es, pues,
inmediato:
Expresa
la masa en gramos de soluto disuelta por cada cien gramos de
disolución. Su cálculo requiere considerar separadamente la masa del
soluto y la del disolvente:
siendo la masa de la disolución la suma de la del soluto y la del disolvente.
Para el estudio de ciertos fenómenos físico-químicos resulta
de interés expresar la concentración en términos de proporción de
cantidad de soluto a cantidad de disolvente. Se emplea entonces la
molalidad: